Convoca a tu Servicio: ¿Cómo ser voluntario para la vacuna contra el COVID-19 en Perú?
Por Elena Miranda | 29 Octubre, 2020
Aún está abierta la convocatoria de la Universidad Peruana Cayetano Heredia para que 4500 voluntarios más se unan a los 7 mil 500 que ya están participando en la prueba de la vacuna contra el COVID-19, elaborada por la farmacéutica china Sinopharm. Este nuevo llamado se dirige a la población con mayor riesgo de contraer el virus, como los trabajadores de salud, miembros de la Policía y de las Fuerzas Armadas, choferes y cobradores de transporte público, trabajadores de mercados y de limpieza pública y otros cuya actividad diaria involucre contacto continuo con el público. Convoca a tu Servicio te informa sobre lo que debes tener en cuenta si quieres inscribirte en línea y participar en los ensayos clínicos.
¿Qué instituciones realizarán los ensayos clínicos para las vacunas chinas contra el COVID-19?
El equipo de investigadores de la Unidad de Ensayos Clínicos de la Universidad Nacional Mayor de San Marcos y del Centro de Estudios Clínicos de la Universidad Peruana Cayetano Heredia lideran, en Lima, la iniciativa conjunta denominada Vacuna COVID Perú, que realiza un estudio experimental con 12 mil voluntarios, que evalúa dos vacunas en la fase III contra el nuevo coronavirus, desarrolladas por China National Biotec Group (CNBG), a pedido de la farmaceútica Sinopharm.
El 30 de agosto, la Universidad Cayetano Heredia inició, a través de Internet, el enrolamiento de 3 mil voluntarios para probar la vacuna. El 27 de setiembre, la Universidad de San Marcos comenzó la inscripción de 3 mil candidatos para los estudios. El 30 de setiembre, la Universidad Cayetano invitó a participar en la investigación a un grupo adicional de 1 mil personas.
El 16 de octubre, la Universidad Cayetano Heredia hizo un llamado a 4500 voluntarios pertenecientes a los sectores más vulnerables a contraer el COVID-19, como los trabajadores de salud, miembros de la Policía y las Fuerzas Armadas, choferes y cobradores de transporte público, trabajadores de mercados y limpieza pública, y otros cuya actividad diaria involucre contacto continuo con el público.
Sin embargo, la inscripción de este grupo fue suspendida temporalmente, debido a que, desde el 19 de octubre, la Universidad de San Marcos convocó a mil personas más del público en general. Debido a que ya concluyó el registro de los voluntarios en dicha universidad, se ha reanudado la inscripción de las personas vulnerables en la Universidad Cayetano Heredia.
Esta guía ha sido elaborada en base a una entrevista con el doctor Germán Málaga, investigador de la Universidad Peruana Cayetano Heredia y uno de los responsables de este estudio experimental, y a la documentación y declaraciones oficiales sobre dichas pruebas.
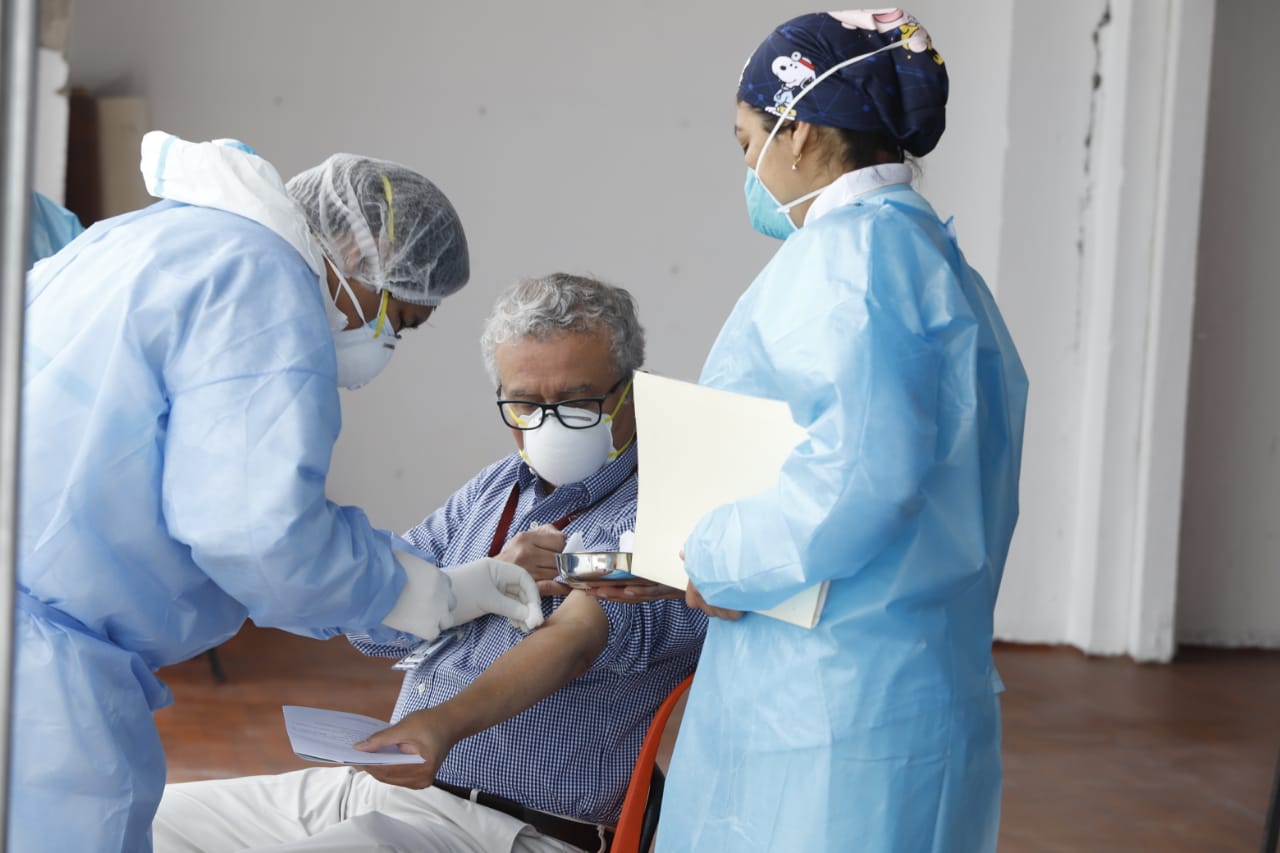
Los voluntarios recibirán dos dosis de la vacuna china contra el COVID-19 y será monitoreados durante 12 meses. Foto: Difusión
¿Qué tipo de vacunas se aplicará a los voluntarios?
La vacuna es un virus que ha sido inactivado, “que está recontra muerto”. Las vacunas que se evaluarán en este estudio provienen de dos cepas, una cepa Wuhan y una cepa Beijing. Se estima que cada una puede tener una inmunidad distinta. Dos mil voluntarios recibirán la cepa Wuhan, dos mil la cepa Beijing y dos mil un placebo. Es decir, de cada tres voluntarios, uno recibe la cepa Wuhan, otro la cepa Beijing y uno un placebo. La investigación evaluará la seguridad (si no causan eventos adversos) y la eficacia (si protegen de la infección).
¿Cuáles son los requisitos para ser voluntario?
-Tener entre 18 años y 65 años de edad.
-Ser peruano o extranjero con arraigo de legalidad en el Perú.
-No tener ninguna enfermedad grave (tuberculosis, enfermedad hepática, pulmonar, cardiaca o renal grave, VIH/sida no controlado o alguna causa de inmunosupresión).
-No tener síntomas agudos de COVID-19 o un diagnóstico reciente del virus.
-No tener alergia o hipersensibilidad a los componentes de la vacuna.
-Las voluntarias no deben estar embarazadas ni dando de lactar.
-Las mujeres deben comprometerse a no embarazarse durante los primeros cuatro meses del estudio y los hombres a no embarazar a una mujer en el mismo periodo de tiempo.
-No estar participando o haber participado en algún estudio de investigación en las últimas semanas.
¿Una persona que ya tuvo COVID-19 puede ser voluntaria?
Sí, a no ser que haya tenido la enfermedad recientemente, lo cual se demuestra con una prueba molecular, o que se sospeche de que la enfermedad está activa.
¿Pueden participar personas con presión alta, diabetes, obesidad u otras enfermedades crónicas?
Hay la capacidad de que las vacunas funcionen para los grupos de personas con presión alta, diabetes, obesidad. Si la hipertensión y otras enfermedades están controladas, no hay ninguna razón para no permitir que se le aplique la vacuna.

En el Perú se están aplicando dos vacunas chinas a los voluntarios durante los ensayos clínicos. Foto: Difusión
Si cumples los requisitos, sigue estos pasos para registrarte como voluntario de las vacunas contra el COVID-19:
Primer paso
-Ingresa a la plataforma web www.vacunacovid.pe
Segundo paso
-Lee la información sobre las vacunas y el estudio experimental.
Tercer paso
-Ingresa al link "Información para participantes"
En esta página encontrarás un enlace de color rojo con la indicación “Deseo participar”, que conduce a un formulario de registro. El registro se cerrará automáticamente cuando se inscriban los mil voluntarios.
💉 CHINA DETALLÓ PLAN PARA APLICAR VACUNA CONTRA EL COVID-19 EN PERÚ 👉 Liu Jingzhen, presidente del laboratorio chino...
Publicado por Convoca en Miércoles, 26 de agosto de 2020
Liu Yang, presidente del Grupo Farmacéutico Nacional de China, en ceremonia en Beijing por ensayos clínicos en Perú. Foto: CGTN
¿Cómo sabré si he sido seleccionado?
En los días siguientes, el equipo de estudio contactará vía telefónica a los mil voluntarios que se registren, quienes deberán confirmar un mensaje de validación, que será enviado a sus correos electrónicos. Luego de verificar sus datos y confirmar que son elegibles para participar, se coordinará con ellos el día y hora en que acudirán al centro de estudio.
¿Se hará público el nombre de los que participen en el estudio?
Los investigadores tienen la obligación de no revelar quiénes participan en el ensayo clínico. La información personal de los participantes será protegida por las instituciones a cargo del estudio, de acuerdo con la Ley de Protección de Datos Personales N.º 29733.
Los investigadores y nuestras instituciones estamos haciendo un esfuerzo para conseguir un arma que controle esta pandemia”. Germán Málaga, investigador de la Universidad Peruana Cayetano Heredia.
¿Dónde están ubicados los centros de vacunación?
Un centro de vacunación se encuentra en el Centro de Investigación Clínica
e Inmunizaciones de la Clínica Universitaria de la Universidad Nacional Mayor de San Marcos, en el campus de la Ciudad Universitaria, en el Cercado de Lima, y otro, en el Centro de Estudios Clínicos de la Universidad Peruana Cayetano Heredia, en San Martín de Porres.
¿Habrá centros de vacunación en otras regiones del Perú?
No, los centros de vacunación solo se encuentran en Lima y los voluntarios deben ser de esta región, para realizarles el monitoreo.
¿Qué debe hacer el voluntario antes de acudir al centro de vacunación?
-Acudir a la cita en el día y la hora indicada, portando el DNI
-Usar vestimenta adecuada: polo, blusa o camisa de manga cero y chompa, abrigo o casaca abierta, que sea fácil de retirar
-No asistir con acompañantes, a excepción de aquellas personas que requieran asistencia
-Utilizar los implementos personales de protección (Mascarilla y protector facial)
¿Qué pasará cuando el voluntario acuda al centro de vacunación?
El día de su cita, el voluntario debe acudir al centro de vacunación elegido, donde debe seguir las señalizaciones e indicaciones predeterminadas. Será evaluado por un médico, que le tomará las funciones vitales, le hará preguntas básicas y verificará que no haya ningún criterio de exclusión. Después, debe firmar dos copias de un consentimiento informado, una de las cuales se llevará. Luego, se le harán algunos exámenes.
¿Qué tipos de exámenes le harán los participantes?
Se les realizará un examen clínico completo. A las mujeres en edad reproductiva, se les tomará una prueba de embarazo. Si es positiva, serán excluidas del ensayo. Si los resultados de las pruebas confirman que la persona es apta como voluntaria, se le aplicará la primera dosis de la vacuna.
¿Cómo se aplicará la vacuna a los voluntarios?
La vacuna se inyecta en el hombro del voluntario. Al término de cada vacunación, deberá reposar por 30 minutos para verificar si hay un efecto inmediato. Antes de retirarse, el personal le dará recomendaciones para su cuidado pues a pesar de ser vacunado, este es un estudio experimental y el voluntario debe seguir tomando precauciones para evitar contraer la infección por el nuevo coronavirus. Luego de 21 días, volverá para la segunda dosis y, después de 28 días, acudirá para tomarse pruebas y que verifiquen si los anticuerpos están presentes o no.

La voluntarios deben firmar un consentimiento informado antes de que se les aplique la vacuna contra el COVID-19. Foto: Difusión
¿Qué es un placebo?
Es una sustancia inactiva que se aplica a los pacientes en los ensayos. Simula ser una vacuna, pero es solo un líquido inofensivo. La aplicación del placebo es aleatoria y tanto el voluntario como el médico desconocen que se le ha sido aplicado pues el líquido viene en el mismo frasco que la vacuna y con la misma etiqueta. Esto se conoce como doble ciego, pues tanto el que aplica como el que recibe no saben si es la vacuna o un placebo.
¿Para qué se aplica un placebo?
El placebo sirve para tener un grupo de control, para comparar los efectos entre las personas que recibieron y no recibieron la vacuna, aunque no lo sepan. Sin un placebo no es posible evaluar cuál es el efecto de la inyección, los efectos adversos e indeseables ni inferir los efectos de protección que da una vacuna. Uno de cada tres voluntarios en este primer ensayo clínico en el Perú recibirá un placebo y no la vacuna contra el COVID-19, es decir, 2 mil de los 6 mil participantes.
¿Qué pasará con los voluntarios que reciban un placebo y no la vacuna?
Los voluntarios a los que se les aplique un placebo tendrán el mismo seguimiento que los que reciban la vacuna. Cuando se compare los síntomas o algún evento o reacción, la única diferencia será la aplicación de la vacuna.
¿Cómo será el monitoreo de los voluntarios?
Desde que se aplica la vacuna, el seguimiento será diario, por teléfono y a través de una aplicación de celular. Los centros de vacunación han contratado a 80 monitores para que se encarguen del seguimiento y estén al tanto de si ocurre algún evento con la persona voluntaria.
¿Cuánto tiempo va a durar el estudio?
La duración total del ensayo clínico es de 16 meses. Sin embargo, el tiempo de seguimiento a los voluntarios es de 12 meses. Sin embargo, los investigadores aclararon que no es necesario esperar este tiempo para tener los primeros resultados del estudio, pues los reportes se emitirán cada tres meses.
¿Los voluntarios recibirán algún pago?
No hay ningún estímulo monetario, pero el estudio sí contempla un presupuesto para el transporte de los participantes y el crédito de la línea del teléfono celular, con el fin de garantizar la comunicación para el monitoreo.
¿Cuáles son los efectos adversos de la vacuna?
En los voluntarios de otros países se han reportado efectos adversos mínimos, como dolor de cabeza, dolores articulares, dolor de cuerpo, fiebre baja, que se ven en todas las vacunas. Esta vacuna, en estructura, es similar a la del sarampión, rubeola y paperas. Aunque es un virus inactivo, puede existir la posibilidad de complicación, si el voluntario hace anafilaxia (reacción alérgica).
¿Hay un seguro que cubre los efectos adversos de la vacuna?
Si hay un efecto adverso atribuible a la vacuna, no al COVID-19, se ha contratado una póliza de seguro médico con la empresa Mapfre, que cubre hasta por 500 mil dólares, para tratar y resarcir esos daños. Así lo establecen las normas que regulan los ensayos clínicos en el Perú. La póliza de seguro vence el 15 de setiembre de 2021.
¿Qué pasará con los voluntarios que no cumplan las indicaciones tras la vacunación o no sigan participando en el estudio?
No están contempladas sanciones para los voluntarios que no cumplan lo estipulado. En los ensayos clínicos hay un riesgo calculado de pérdida. La persona, en cualquier momento, podría decidir no seguir participando, lo cual es parte de las contingencias que pueden ocurrir en el estudio. Si cambian de teléfono o pierden el contacto con los monitores, estos harán lo posible por encontrarlos.
¿El laboratorio Sinopharm cuenta con todas las autorizaciones de salud para iniciar los ensayos clínicos?
El Comité Nacional Transitorio de Ética en Investigación para la evaluación y supervisión ética de los Ensayos Clínicos de la enfermedad Covid-19 (CNTEI-COVID19) ha participado en el proceso para otorgar la autorización como patrocinador del estudio a la Universidad Peruana Cayetano Heredia. Dicho ensayo es supervisado por este grupo y por la Oficina General de Investigación y Transferencia Tecnológica (OGITT) del Instituto Nacional de Salud (INS), según se señala en la plataforma web.
¿Quiénes conforman el equipo que realiza los ensayos clínicos de la vacuna china en el Perú?
Para la logística y conducción del ensayo en el Perú, todos son peruanos de Universidad Peruana Cayetano Heredia, que han sido capacitados por un equipo de científicos de la farmacéutica Sinopharm, de China. Este mes, una delegación de científicos chinos llegó a nuestro país, con el lote de vacunas, para acompañar el proceso de los ensayos clínicos.
¿Cómo se financian los ensayos clínicos?
China National Biotec Group Company Limited está financiando la investigación, para el equipamiento de las universidades de San Marcos y Cayetano Heredia, con el fin preservar las vacunas y las muestras, capacitar al personal e implementar las plataformas necesarias.
¿Cada cuánto tiempo van a emitir informes sobre el estudio?
Los investigadores tienen la obligación de reportar periódicamente al Instituto Nacional de Salud (INS) el avance, en cuanto al tema de seguridad. En cuanto a los temas de efectividad, no va a ser posible, por el tema de doble ciego (aplicación de un placebo). También deben reportar a esta institución todos los efectos adversos en tiempo real.
¿Se realizarán ensayos clínicos de otros laboratorios?
Ocho laboratorios están en la carrera de fase 3 y han solicitado hacer ensayos clínicos en el Perú. Tres de ellos han sido autorizados (Sinopharm, de China, Curevac AG, de Alemania, y Astrazeneca, de Reino Unido).
¿Qué pasará cuando concluyan los ensayos clínicos?
Al terminar la fase 3 de los ensayos clínicos, las vacunas no van a estar disponibles inmediatamente. Se deben publicar los resultados y, luego, se debe pasar por un proceso regulatorio.
Foto principal: DIfusión

 Menú
Menú
 Buscar
Buscar





 Sé el primero en leer nuestras publicaciones
Sé el primero en leer nuestras publicaciones