Debido a la insuficiente información sobre los ensayos clínicos y al alto costo de la candidata a vacuna contra el COVID-19 de la compañía británica AstraZeneca, el Gobierno peruano no firmará un convenio con dicha farmacéutica para la compra de estos productos. Esta decisión coincide con la noticia del fallecimiento de un voluntario del estudio experimental en Brasil, que se suma a los efectos adversos registrados por otros dos participantes de la investigación en el Reino Unido. Aunque AstraZeneca obtuvo la autorización para realizar pruebas en nuestros país, el inicio de estas fue supeditado a la reanudación de las investigaciones en los Estados Unidos, cuya autoridad regulatoria evalúa lo ocurrido con los voluntarios.
Actualización: 22 de octubre
El Gobierno peruano decidió no firmar un convenio vinculante con el laboratorio AstraZeneca, del Reino Unido, debido a la insuficiente información sobre los ensayos clínicos de su candidata a vacuna contra el COVID-19, reveló ayer la ministra de Salud, Pilar Mazzetti, ante ante la Comisión de Salud y Población del Congreso de la República
“Nosotros podemos tener mucha preocupación por tener una vacuna. Todos los países están dispuestos a correr cierto riesgo frente a una vacuna de emergencia, pero tampoco podemos correr mucho riesgo”, afirmó Mazzeti.
AstraZeneca ya tiene la autorización de las autoridades peruanas para realizar los ensayos clínicos con voluntarios en nuestro país, pero estaban supeditados a la reanudación de las pruebas en los Estados Unidos. Tras la decisión del Gobierno peruano de no firmar un acuerdo con la farmacéutica, aún no se sabe si el Instituto Nacional le revocará el permiso.
La titular de Salud recordó que el laboratorio que desarrolla la vacuna con la Universidad de Oxford ya registraba dos casos de la enfermedad mielitis transversa en voluntarios de sus ensayos clínicos desarrollados en el Reino Unido y que ayer se conoció que un voluntario de esta vacuna experimental falleció en Brasil, aunque no se ha informado si recibió la vacuna o un placebo.
Mazzetti informó que el último martes se reunió con el premier Walter Martos y el canciller Mario López para analizar la decisión de la comisión de trabajo multisectorial encargada de la adquisición de las vacunas contra el coronavirus, y todos coincidieron en que no se podía suscribir un acuerdo con AstraZeneca, debido a la escasa información con la que se contaba.

La ministra de Salud y diversos expertos acordaron se reunieron para tratar la compra de vacunas contra el coronavirus al laboratorio AstraZeneca. Foto: Difusión
Según la agencia Reuters, el premier Walter Martos explicó que el Gobierno peruano solicitó a AstraZeneca los avances de sus estudios sobre la repercusión de sus posibles vacunas, propiedades y especificaciones, pero que hasta esta semana no le envió dicha información. Además, la farmacéutica ofrecía cantidades mínimas de inoculación.
“Nos estaban ofreciendo una cantidad muy poca de vacunas para el país en comparaciones de otros laboratorios que nos están ofreciendo grandes cantidades a menores costo”, dijo Martos en una conferencia con la prensa extranjera realizada este 22 de octubre. Agregó que el laboratorio quería un adelanto económico bastante significativo “con el riesgo de no recuperarlo” porque si no se obtenía la vacuna, se perdía el dinero adelantando.
Dos laboratorios ya realizan ensayos en Perú
Con la suspensión de los ensayos clínicos de la vacuna contra el COVID-19 del laboratorio estadounidense Johnson & Johnson, el 12 de octubre, y la compañía británica Astrazeneca, el 7 de setiembre pasado, ya son dos las farmacéuticas que retrasan el inicio de sus estudios experimentales en el Perú por reacciones adversas en los voluntarios de otros países. Por hora, solo están realizando pruebas con participantes peruanos las farmacéuticas Sinopharm, de China, y Curevac, de Alemania.
En un comunicado, Johnson & Johnson informó que detuvo temporalmente todos sus ensayos clínicos de la vacuna que está siendo desarrollada por Janssen Pharmaceutical Companies, incluido del ensayo Ensemble de fase 3, "debido a una enfermedad inexplicable en un participante del estudio". "La enfermedad del participante está siendo revisada y evaluada por la Junta de Monitoreo de Seguridad de Datos (DSMB) independiente de ENSEMBLE, así como por nuestros médicos internos clínicos y de seguridad", señaló.
El 9 de octubre pasado, el ministro de Relaciones exteriores de Perú, Mario López, adelantó que este mes Johnson & Johnson empezaría los ensayos clínicos de su vacuna en el Perú con la convocatoria de voluntarios. Sin embargo, aún está pendiente la autorización del Instituto Nacional de Salud (INS), que hizo observaciones al expediente presentado por el patrocinador del estudio.
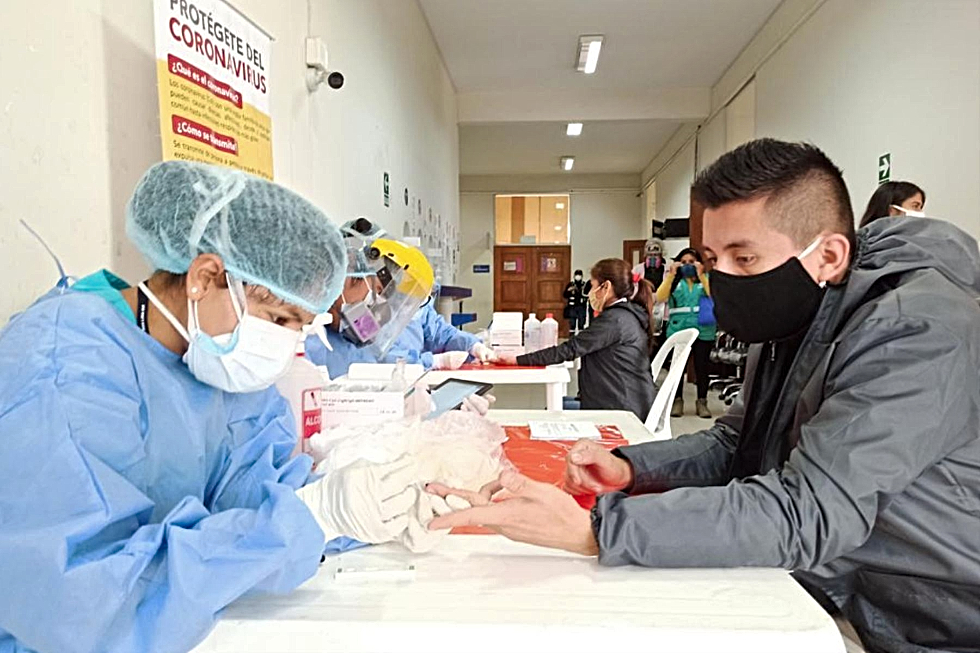
El Perú es uno de los países que registra mayor número de casos de contagios y muertes por el nuevo coronavirus. Foto: Andina
Por el momento, tres farmacéuticas extranjeras están autorizadas para realizar los ensayos clínicos de sus vacunas contra el COVID-19 en el Perú, pero solo dos han enrolado a voluntarios. La primera fue el gigante farmacéutico chino Sinopharm que, desde el 9 de setiembre, está aplicando dos cepas del virus inactivado a 7 mil voluntarios, y la segunda, la compañía biofarmacéutica alemana Curevac AG, que comenzó a aplicar las dosis a 271 voluntarios.
A pesar de que el 17 de setiembre la compañía biofarmacéutica AstraZeneca AB, con sede en Reino Unido, obtuvo la autorización del Instituto Nacional de Salud (INS) para realizar el ensayo clínico de su vacuna contra el COVID-19 en el Perú, no ha comenzado el enrolamiento de los 5 mil voluntarios que requiere, en una primera etapa, y de los otros 5 mil, para una segunda.
Convoca.pe consultó al Ministerio de Salud si tras la decisión de no firmar el convenio con Astrazeneca, se le revocará la autorización para realizar los ensayos clínicos en el Perú. Sin embargo, aún no dan respuesta a esta interrogante.
Los estudios experimentales de Sinopharm y de AstraZeneca se encuentran en la fase 3, que evalúa la eficacia y la seguridad de la vacuna, mientras que el de Curevac está en la fase 2, que busca determinar la eficacia, priorizando la respuesta del sistema inmunitario.
Ensayos de AstraZeneca en Perú en suspenso
El proceso de autorización para los ensayos clínicos de la vacuna de AstraZeneca en el Perú demoró un mes, pues dicha compañía presentó su solicitud al INS el 18 de agosto de 2020. El procedimiento fue observado dos veces, el 22 de agosto y el 11 de setiembre. En ambos casos, las observaciones fueron absueltas por el patrocinador, días después.
Sin embargo, el 17 de setiembre, AstraZeneca envió un correo electrónico al INS, informando que, voluntariamente, había decidido pausar el enrolamiento del estudio, el 6 de setiembre, debido a un "SUSAR" reportado en el objeto de estudio, lo que provocó que la Administración de Medicamentos y Alimentos (FDA) de Estados Unidos dispusiera la pausa de dicho estudio el 7 de setiembre.
Convoca.pe tuvo acceso a la Resolución Directoral 391-2020-OGITT-INS, que otorgó el 17 de setiembre la autorización a AstraZeneca para su estudio experimental en el Perú. Dicho documento señala en sus considerandos que “No se enrolará ningún paciente en el estudio hasta que la FDA confirme el levantamiento de la pausa, posterior a la revisión del comité de monitoreo de seguridad de datos relacionados a la vacuna”. La fecha estimada del inicio del enrolamiento de voluntarios, el 10 de setiembre, se ha postergado hasta nuevo aviso.

En la resolución del INS figura que AstraZeneca no comenzará ensayos hasta que obtenga el permiso de la FDA, de los Estados Unidos.
Investigan efectos adversos de vacuna de AstraZeneca
El ensayo clínico que realizará AstraZeneca en el Perú forma parte de un estudio de fase 3, con 30 mil voluntarios, centrado en Estados Unidos y que también considera a Chile, con el fin de probar la vacuna AZD1222, elaborada por la Universidad de Oxford y la empresa de biotecnología Vaccitech. Los dos países latinoamericanos han sido elegidos debido a las altas tasas de transmisión del virus.
El enrolamiento de voluntarios para la vacuna de AstraZeneca, a nivel mundial, comenzó el 17 de agosto. El 7 de setiembre, los estudios experimentales de AstraZeneca se detuvieron temporalmente en todo el mundo para que un comité independiente revise los datos de seguridad de una enfermedad inexplicable que apareció en una voluntaria del Reino Unido, según informó la farmacéutica.
La persona afectada fue una mujer británica de 37 años, que sufrió de “mielitis transversa”, luego de recibir la segunda dosis de la vacuna de coronavirus, a fines de agosto, según un reporte interno de AstraZeneca, al que CNN tuvo acceso. Esta enfermedad neurológica tiene que ver con la inflamación de la médula espinal.
El informe reveló que, el 2 de setiembre, mientras corría, la mujer tuvo un tropiezo pero no se cayó. Al día siguiente, presentó dificultad para caminar, dolor y debilidad en los brazos, disminución de la sensibilidad y dolor en el torso, dolor de cabeza y dificultad para usar sus manos. El 5 de setiembre, la voluntaria fue hospitalizada.

Científicos de AstraZeneca reanudaron ensayos clínicos en Reino Unido, Japón, Sudáfrica, India y Brasil. Foto: Difusión / AstraZeneca
El 12 de setiembre, los estudios con voluntarios se reanudaron en Inglaterra y Brasil, tras la confirmación de la Autoridad Reguladora de la Salud de Medicamentos (MHRA) de que era seguro hacerlo. Posteriormente, se reiniciaron en Sudáfrica, India y Brasil. Aún no se retoman en los Estados Unidos porque la FDA está revisando la información sobre el caso de la voluntaria, para tomar una decisión.
Ha pasado un mes desde la suspensión temporal de los ensayos clínicos de AstraZeneca en Estados Unidos. Al ser consultado por los medios de comunicación de dicho país, el 30 de setiembre pasado, el comisionado de la FDA, Stephen Hahn, dijo que no podía hablar de “información comercial confidencial”. El 1 de octubre se conoció que la FDA amplió la investigación sobre el caso.
El 2 de octubre, AstraZeneca informó que reanudó los ensayos clínicos en Japón tras obtener el visto bueno de la Agencia Japonesa de Productos Farmacéuticos y Dispositivos Médicos (PMDA). Además, la compañía recordó que continúa trabajando con la FDA, para facilitar la revisión de la información necesaria para tomar una decisión con respecto a la reanudación del ensayo en Estados Unidos.
La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil informó que el 19 de octubre le notificaron la muerte de un hombre de 28 años, proveniente de Río de Janeiro, que era voluntario en los ensayos clínicos de AstraZeneca. Aunque la farmaceútica no se pronunció, la Universidad de Oxford emitió un comunicado en el que señala que, tras una cuidadosa evaluación, no encontró problemas de seguridad y que continuará con los estudios experimentales.
AstraZeneca solicitó probar vacuna en clínicas de Lima
Aunque la empresa AstraZeneca AB patrocinará y financiará el ensayo clínico de la vacuna en el Perú, la ejecución está a cargo de la empresa Iqvia RDS Perú S.R.L. y el centro de investigación responsable del estudio es el Policlínico Especializado en Neurología S.A.C. y su Centro de Investigaciones Médicas, ubicado en el distrito de La Perla, en el Callao. El investigador principal es Sergio Recuenco Cabrera.
Además del Policlínico Especializado en Neurología, la vacuna de AstraZeneca también se aplicará a los voluntarios en el Centro de Investigaciones Ricardo Palma, a cargo del doctor Juan Guanira Carranza; en la Unidad de Investigación de la Clínica Internacional, bajo la responsabilidad del doctor Alfredo Guerreros Benavides; en el Hospital Central de la Fuerza Aérea del Perú, a cargo de la doctora María Carmela Faverio Manucci; y en la Unidad de Investigación de Enfermedades Respiratorias de la Clínica San Pablo, con el doctor Armando Daniel Luza Salazar.
El nombre de estas clínicas donde también se aplicará la vacuna a los voluntarios figura en la resolución del INS que autoriza el estudio experimental y anexa el formulario con los centros de investigación donde se usarán los productos y suministros del ensayo clínico.
Los 271 voluntarios para el estudio de Curevac en Perú no han sido convocados de manera pública sino que son personas allegadas a los centros de investigación”. Gloria Niño de Rivera, vocera de Curevac.
Los participantes del estudio de AstraZeneca en el Perú serán adultos de 18 a 64 años y, por lo menos, 25% serán adultos mayores de 65 años. Una parte de los 10 mil voluntarios recibirá una dosis de la vacuna AZD1222 y otra, un placebo (Solución de cloruro de sodio), pues el ensayo es de tipo doble ciego. Después de la aplicación de la primera dosis de la vacuna, se deberá esperar cuatro semanas para poner la segunda. El estudio dura 24 meses y a los voluntarios se les hará seguimiento durante 23 meses.
Para el ensayo clínico de la vacuna de AstraZeneca, el patrocinador ha contratado un seguro con la empresa Rímac Seguros que cubra los posibles daños y perjuicios a los participantes del estudio experimental. Convoca solicitó al INS el monto de la póliza, pero la entidad se negó a brindar dicha información porque considera que este dato "es de propiedad del patrocinador del estudio y no puede ser compartido con personas ajenas a la autoridad reguladora, que es el INS".
Independientemente del seguro contratado, AstraZeneca, como patrocinador, tiene la obligación de otorgar una indemnización por el daño que un sujeto de investigación pueda sufrir en el Perú, como consecuencia del uso del producto en investigación o por un procedimiento o intervención realizado con el propósito de la investigación. Así lo establece el Reglamento de Ensayos Clínicos, aprobado por el Decreto Supremo N° 021-2017-SA.
Curevac ya prueba su vacuna en Perú
Desde el 28 de setiembre pasado, la compañía biofarmacéutica alemana Curevac está aplicando la vacuna contra el COVID-19 a voluntarios en el Perú, en la sede del Instituto de Investigación Nutricional, en La Molina. El investigador a cargo es el doctor Claudio Lanata de las Casas.
Los 271 voluntarios que Curevac requiere para este estudio de fase 2 en nuestro país no han sido convocados de manera pública, sino que son personas allegadas a los centros de investigación, que se van enrolando, informó Gloria Niño de Rivera, vocera de Curevac, desde su sede en México, en diálogo con Convoca.pe.
La representante de la farmacéutica indicó que los ensayos de fase 1 de la vacuna de Curevac se han realizado en Alemania y Bélgica. A fines de setiembre, se han iniciado las pruebas de fase 2 en Panamá y Perú, con un total de 690 participantes: adultos mayores de 61 años o más y adultos de 18 a 60 años.

La vacuna de Curevac se probó en Alemania y Bélgica y, desde setiembre, en Perú y Panamá. Foto: Difusión / Curevac
Los voluntarios reciben dos dosis de la vacuna CVnCoV, con 28 días de diferencia entre cada una. El estudio dura 13 meses y el tiempo de seguimiento a los participantes será de 180 días.
"Este estudio tiene como objetivo confirmar la selección de la dosis para nuestra vacuna candidata y proporcionar más evidencia de que podemos proporcionar una vacuna segura y bien tolerada a los adultos mayores que tienen un mayor riesgo de COVID-19", señaló en un comunicado Mariola Fotin-Mleczek, directora de tecnología de Curevac.
Para el ensayo clínico de la vacuna, Curevac ha contratado un seguro con la empresa Chubb Seguros Perú S.A.C. que cubra los posibles daños y perjuicios a los participantes del estudio experimental. Al igual que con AstraZeneca, Convoca.pe solicitó al INS el monto de la póliza, pero esa entidad se negó a brindar dicha información. Independientemente del seguro contratado, el patrocinador debe otorgar una indemnización por el daño que un sujeto de investigación pueda sufrir en el Perú.
Curevac estima que comenzará la fase 2b/3 del ensayo clínico global en el cuarto trimestre de este año, con hasta 30 mil participantes de diversos países.

 Menú
Menú
 Buscar
Buscar


 Sé el primero en leer nuestras publicaciones
Sé el primero en leer nuestras publicaciones